- Что такое грибок волос и как лучше от него избавиться
- Что представляет собой грибок
- Как проявляет себя грибок кожи головы: наиболее распространенные симптомы
- Основные симптомы себореи
- Признаки трихофитии
- Симптоматика микроспории
- Особенности диагностики грибка волос
- Как правильно лечить грибок волос
- Грибок дрожжевой лечение народными средствами
- Современные представления о грибковой патологии пищеварительного тракта
- Диагностика
- Кандидоз
- Классификация кандидоза
Что такое грибок волос и как лучше от него избавиться

Размножаясь спорами, грибок легко переносится по воздуху или контактно-бытовыми путем. При этом споры очень «живучие» — они долго сохраняются на одежде, постельном белье, предметах гигиены и в любой момент готовы активизироваться.
Что делать, чтобы предотвратить заселение патологическими микроорганизмами и как вылечить грибок волос, чтобы заболевание не возвращалось снова и снова – разбираемся с симптоматикой, диагностикой и особенностями терапии.
Что представляет собой грибок

Грибы по своей сути – это гетеротрофы, то есть для своего питания они используют готовые органические вещества. Их пищеварение – внешнее. Это означает, что все продукты жизнедеятельности грибков попадают на кожные покровы и слизистые оболочки человека. Формируя целые колонии, они проникают в эпидермис и провоцируют воспаление. При этом здоровые клетки гибнут, в том числе и волосяной фолликул, который зачастую восстановить после успешного лечения уже не удастся.
Как проявляет себя грибок кожи головы: наиболее распространенные симптомы
Причиной зуда, шелушения (перхоти), потери волос очень часто является именно грибок (микоз). Наиболее часто волосистую часть головы заселяют:
- Microsporum: становятся причиной микроспории;
- Trichophyton: являются возбудителями трихофитии (стригущего лишая);
- Malassezia furfur: приводят к себорее.
Каждая из инфекций будет проявлять себя по-разному, однако можно выделить некоторые самые распространенные тревожные симптомы — одновременное проявление двух и более должно насторожить каждого человека:
- внезапное ухудшение общего состояния волос: стали сухими, тусклыми, стали обильно выпадать;
- появилась перхоть (при том, что ранее такого не наблюдалось), и/или ее количество возрастает;
- появились отдельно локализованные шелушащиеся участки;
- образовываются залысины и проплешины, которые быстро разрастаются;
- на коже головы обнаружились ранки, корочки, бугорки непонятного происхождения;
- волосы становятся ломкими у основания фолликула, вследствие чего появляются черные точки на коже.
Микозы на ранней стадии себя не обнаруживают, поэтому следует быть очень внимательными, и при появлении какого-либо симптома незамедлительно обращаться к специалисту. Проблемами волосяной части головы занимаются врачи-трихологи или дерматологи.
Основные симптомы себореи

Характерным признаком являются корочки (поверхностный слой кожи растрескивается, отслаивается), а также обильная перхоть. Могут появиться красновато-розовые пятна. Больные отмечают ощущение стянутой кожи и зуд, когда на кожу головы попадает холодная вода.
Себореей чаще всего болеют дети грудного возраста и подростки.
Признаки трихофитии
Пожалуй, наиболее тяжелый вид микоза кожи головы в зоне роста волос, вследствие которого больной теряет волосяной покров. Дифференцируют поверхностную и глубокую формы.
При поверхностной трихофитии сначала можно обнаружить шелушащиеся очаги, ломкость волос у основания фолликулов, вследствие чего кожа головы покрывается черными точками. На остатке волоса после слома можно заметить серый налет. Зоны поражения могут приобретать красный оттенок, зудеть, отекать.

Симптоматика микроспории
Споры Microsporum распространяются чрезвычайно быстро. Симптоматика имеет много схожего с поверхностной трихофитией, поэтому исключить последнюю можно лишь с помощью лабораторного исследования. Так же как и в случае стригущего лишая, обнаруживаются круглые пятна, которые шелушатся, могут появляться гнойные корочки. Волосы становятся очень ломкими. В отличие от трихофитии, ногти в данном случае не поражаются.
Особенности диагностики грибка волос
Определить наличие и разновидность грибка специалист сможет относительно легко и достоверно с помощью лабораторных исследований путем применения микроскопического и культурального методов. Первый предполагает взятие у больного волос и чешуек кожи с целью исследования на предмет наличия спор мицелия, пузырьков газа, фрагментов крупных грибов. Культуральный метод используется, если присутствие грибка все-таки обнаруживается и позволяет определить конкретный тип мицелия, заселившего волосяную часть головы больного. Для этого обнаруженный грибок выращивается в питательной среде, после чего выросшая колония исследуется, в частности оценивается характер роста (процесс занимает несколько дней).
Одно из современных средств, используемых для определения микоза, – лампа Вуда. Устройство излучает волну определенной длины и позволяет подсветить колонии, давая представление о масштабах и локализации, но не предоставляя ответ относительно вида микроорганизма, а значит и тактики лечения.
Как правильно лечить грибок волос
Как уже было отмечено, человек обнаруживает грибок, когда тот уже успел «обосноваться» в волосах. Как и любое заболевание, микоз на более поздней стадии лечить значительно сложнее и полагаться в этом вопросе на народные методы – значит рисковать драгоценным временем.
Тактика лечения определяется специалистом, исходя из таких данных, как глубина и площадь очагов, вид грибка, общее состояние организма, анамнез пациента. Лечение, как правило, комплексное и включает системные препараты и наружные средства (например, прием таблеток и использование мазей). Также может быть назначена иммунотерапия или витаминотерапия, ведь грибок развивается «с позволения» иммунитета.
Микозы успешно лечатся – на сегодняшний день существуют эффективные противогрибковые препараты. Однако грибковую инфекцию лечить значительно сложнее, чем бактериальную – клетки гриба очень схожи по строению с клетками человека. Если в случае антибактериальной терапии о результатах можно судить уже на вторые сутки, то в случае с микозом – лишь на седьмые. После стихания клинических проявлений еще в течение 2-х недель важно принимать противогрибковые препараты. Таким образом, лечение требует времени и терпения — может потребоваться от 3-х недель. Но ни в коем случае нельзя останавливаться, как только появились результаты – это однозначно приведет к рецидиву, а новые колонии могут оказаться уже более устойчивыми к используемому препарату.
Дерматомикозы далеко не всегда являются самостоятельными заболеваниями. Зачастую они спровоцированы другими болезнями. Грамотный врач-трихолог сможет не только назначить эффективный курс лечения, который позволит избавиться от грибка волос как можно скорее, но и сможет заподозрить первопричину микоза, тем самым обеспечив выявление заболевания на более ранней стадии.
Вывод прост: чтобы избавиться от грибка волос, лучше всего отправиться на прием к врачу-трихологу, который безошибочно определит вид микоза и назначит лечение. Не стоит заниматься самолечением, оставляя колониям патогенных микроорганизмов хоть малейший шанс на выживание. Кроме того, следует принять во внимание тот факт, что противогрибковые препараты оказывают серьезное влияние на печень, поэтому лечиться такими медикаментами можно только по назначению и под контролем специалиста, который поможет выбрать наиболее щадящую и при этом эффективную тактику лечения.
Источник
Грибок дрожжевой лечение народными средствами
Грибы вызывают широкий спектр заболеваний — от кожных дерматофитных инфекций до тяжёлых заболеваний у пациентов со сниженным иммунитетом. Причиной микозов могут быть как дрожжевые, так и нитевидные формы грибов.
Грибы рода Candida, широко распространённые в окружающей среде, входят в состав условно-патогенной микрофлоры кожи, желудочно-кишечного тракта и женских половых органов. Их чрезмерное размножение, возникающее вследствие антибактериальной терапии, может привести к развитию инфекционных заболеваний.
Наиболее подвержены микозам пациенты с иммунодефицитами. Возбудитель большинства грибковых инфекций — С. albicans. Другие виды, такие как С. tropicalis, С. parapsilosis, С. glabrata и С. pseudotropicalis, представляют опасность для пациентов со сниженным иммунитетом, так как они устойчивы к действию большинства противогрибковых препаратов.
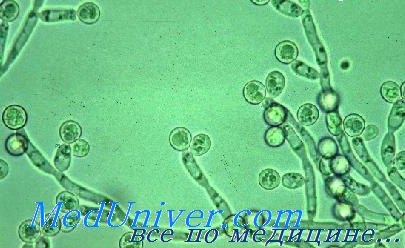
Патогенез инфекции дрожжевых грибов. Несмотря на то что грибы имеют факторы адгезии, экстрацеллюлярные липазы и протеазы, они обладают достаточно слабой инвазивностью. Инфекция обычно возникает при нарушении баланса нормальной микрофлоры (при применении антибиотиков) или снижении иммунитета.
Клинические признаки инфекции дрожжевых грибов. Кандидозы обычно сопровождаются болью, зудом и образованием творожистого налёта на поверхности слизистых оболочек, при удалении которого возникает кровоточивость. Часто возникает поражение кожи и ногтевых пластин. У пациентов со сниженным иммунитетом развивается тяжёлый фарингит и эзофагит, сопровождающийся дисфагией и снижением массы тела (часто наблюдают у больных СПИДом).
При нейтропении возникают системные микозы. Кроме того, на фоне применения антибиотиков широкого спектра действия в отделениях интенсивной терапии грибы рода Candida могут вызывать генерализованные и катетер-ассоциированные инфекции.
Лабораторная диагностика инфекции дрожжевых грибов. Поскольку грибы рода Candida — представители нормальной микрофлоры, их культивирование и выделение оправдано только на фоне уже сложившейся клинической картины. Они хорошо растут на обычных питательных средах. Методы диагностики — микроскопия, молекулярные методы исследований (у пациентов со сниженным иммунитетом), биохимические методы или секвенирование 18S рибосомальной РНК (для видовой идентификации).
Чувствительность инфекции дрожжевых грибов к препаратам. Большинство грибов чувствительны к амфотерицину В (за исключением С. lusitaniae). Кроме того, терапевтическим эффектом обладают производные имидазола (флуконазол) и 5-флуцитозин. При кандидемии рекомендовано назначение каспофунгина.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Современные представления о грибковой патологии пищеварительного тракта
В гастроэнтерологии, как и в других областях медицины, динамично развиваются методы диагностики и лечения грибковых инфекций на основе изучения физиологии, микробиологии, фармакологии, молекулярной патологии и медицинской генетики. Детально изучаются уже
В гастроэнтерологии, как и в других областях медицины, динамично развиваются методы диагностики и лечения грибковых инфекций на основе изучения физиологии, микробиологии, фармакологии, молекулярной патологии и медицинской генетики. Детально изучаются уже известные варианты болезни и описываются редкие и новые нозологические формы.
Грибы, являясь нормальными комменсалами желудочно-кишечного тракта (ЖКТ), становятся патогенными при определенных условиях. Это касается в основном дрожжеподобных грибов Candida spp., виды и даже штаммы которых различаются по факторам агрессии, способности к адгезии и инвазии [15].
Candida albicans — наиболее частый возбудитель кандидоза ЖКТ. Однако в последние годы большую роль играют Candida non-albicans (C. krusei, C. tropicalis, C. kefyr, C. glabrata, C. parapsilosis); у лиц с иммунодефицитом их пропорция составляет более 50%, при «относительно нормальном» иммунитете — 15%.
Грибы Candida (условно-патогенные микроорганизмы) заселяют ЖКТ — этот феномен называется колонизацией, — процесс протекает бессимптомно. Исследование взрослых здоровых добровольцев показало, что Candida albicans присутствует в орофарингеальной зоне у 20–30% из них, в тонком кишечнике — у 50–54%, в толстом кишечнике — у 55–70% и в фекалиях — у 65–70% [9, 13]. При исследовании состава микрофлоры полости рта у населения нескольких стран Европы обнаружено присутствие грибов у 10–25% людей, в кале — у 65–80% [11, 17]. Детально изучена колонизация зева грибами Candida у больных гемобластозами: она составила 33% [8]. В биоптатах гастродуоденальных язв в 17–30% случаев находят дрожжеподобные грибы [12]. У 50% жителей Германии в микробиоте кишечника присутствуют грибы, а у онкогематологических больных колонизация кишечника составляет 63–65% [10, 11]. Нельзя забывать, что у 0,8–4% пациентов грибы случайно обнаруживаются в пузырной и протоковой желчи, а при желчнокаменной болезни — у 15–20%.
Бессимптомное пребывание грибов в ЖКТ может прекратиться, когда они приобретают патогенные свойства. Так, у больных с нейтропенией грибы из кишечника могут диссеминировать в печень, селезенку и легкие, а в катетер-ассоциированной ситуации грибы попадают непосредственно в ток крови, достигают сердца и почек.
Дрожжеподобный гриб Cryptococcus neoformans в патологии ЖКТ как этиологический фактор играет незначительную роль. Он чаще поражает нервную систему и, диссеминируя из первичного очага, вовлекает гастроинтестинальный тракт. Описаны единичные случаи (чаще посмертно) криптококкового эзофагита, стоматита, терминального илеита, колита, холецистита, панкреатита. Как правило, они относились к ВИЧ-серопозитивным больным, а также к пациентам, страдающим гипергаммаглобулинемией Е с рецидивирующими абсцессами печени и перианальной зоны.
Болезни ЖКТ, вызванные диморфными патогенными грибами (II группы патогенности), зарегистрированы в Южной Америке, но время от времени встречаются как спорадические случаи по всему миру. Большинство диморфных грибов в природе существуют в мицелиальной форме, попав в организм они трансформируются в дрожжеподобные и приобретают патогенные свойства. Пероральный путь проникновения не характерен, в ЖКТ эти грибы попадают при диссеминации из других органов. Blastomyces dermatitidis продуцирует гранулематозное повреждение в желудке и тонком кишечнике. Coccidioides immitis, Histoplasma capsulatum, Paracoccidioides brasiliensis и Sporothrix schenckii поражают кишечник только при диссеминации из кожных очагов и респираторного тракта [6, 15].
Грибы Aspergillus spp. редко вызывают болезнь ЖКТ, только в случаях стойкой нейтропении, кахексии и при других отягощающих состояниях.
Грибы класса Zygomycetes могут привести к развитию интестинального зигомикоза, который, как правило, ассоциирован с амебиазом, голоданием, диабетическим кетоацидозом, почечным гемодиализом. Penicillium spp. и Geotrichum поражают ЖКТ также редко.
Дрожжеподобные, плесневые и некоторые диморфные грибы — это условно-патогенные, оппортунистические микроорганизмы, которые широко распространены в окружающей среде и легко могут попадать на кожу, слизистые оболочки полости рта, гениталий и в дыхательные пути. Кроме того, для грибов характерен эндогенный способ существования (миконосительство).
ЖКТ покрыт слизистой оболочкой, состоящей из двух компонентов — поверхностного скользкого, слизистого слоя, по которому микроорганизмы легко продвигаются вдоль всего ЖКТ, и более глубокого плотного гликопротеинового слоя с остатками сиаловой кислоты, который формирует физиологический барьер. Адгезия и последующая инвазия грибов через этот плотный слой возможны только благодаря продукции грибами протеолитических «ферментов инвазии»: коагулазы, каталазы, козеиназы, фосфолипазы, а также фибриллярных протеиновых комплексов и эндотоксинов [15].
При физиологическом благополучии между макро- и микроорганизмами существует определенное равновесие, в котором играют роль, с одной стороны, факторы устойчивости организма к микроскопическим грибам, а с другой — факторы патогенности грибов.
Устойчивость организма зависит от принадлежности к группам риска и состояния иммунной системы.
Перечислим факторы риска развития грибковых инфекций ЖКТ.
- Поражение слизистых оболочек полости рта (красный плоский лишай, зубные протезы, травмы, ксеростомия, использование гормональных ингаляторов).
- Хронические заболевания ЖКТ (атрофический гастрит, гипоацидность желудка, ахалазия, бульбит, эрозивно-язвенные заболевания пищевода и кишечника, дивертикулез, полипоз, гастроэзофагальная рефлюксная болезнь, энтероколит, болезнь Крона, синдром раздраженной кишки, обсемененность желудка Helicobacter pylori, дисбиоз, микст-инфекция кишки).
- Травмирование слизистой оболочки (ожоги, пищеводно-желудочный зонд, эндотрахеальная интубация).
- Беременность.
- Период новорожденности (недоношенность, массивность инфекции при прохождении через родовые пути, естественное несовершенство иммунной системы).
- Пожилой возраст (старение иммунной системы, сопутствующие заболевания, уменьшение амплитуды продольных сокращений пищевода, силы сокращений сфинктеров, нарушение процессов всасывания и т. д.).
- Онкологические и гематологические заболевания (нейтропения).
- Эндокринопатии (особенно сахарный диабет).
- СПИД, ВИЧ-инфицированность.
- Трансплантационные операции.
- Состояния, требующие пребывания в отделениях интенсивной терапии.
- Тяжелые аллергические заболевания.
- Прием антибиотиков, цитостатиков, гормонов и других химиопрепаратов в неадекватных дозах.
- Нарушения питания, в том числе голодание с целью снижения веса.
- Алкоголизм, курение, наркомания.
Важным компонентом защиты от инвазии ЖКТ является иммунная система, ассоциированная с кишечником. Клеточная часть этой системы включает в себя интраэпителиальные лимфоциты, которые препятствуют дисперсии возбудителя через lamina propria и агрегации в пейеровых бляшках. В-лимфоциты кишечника участвуют в продукции секреторных IgA и IgM, которые уменьшают способность грибов к адгезии.
Т-клетки здорового организма продуцируют защитный интерферон, усиливают фагоцитоз, активируют Т-цитотоксические лимфоциты. СД4 и СД8 укрепляют местный иммунитет в ЖКТ. Причем оказалось, что цитотоксичность СД8 играет более существенную роль в предотвращении заболевания, чем предполагали раньше.
В защите важны также макрофагальный и нейтрофильный фагоцитоз, препятствующие диссеминации грибковой, особенно кандидозной инфекции.
У ВИЧ-пациентов и больных с нейтропенией, у которых фагоцитоз резко подавлен, местная инвазия и диссеминация инфекции наступают очень быстро. Известно, что нейтрофилы хотя и не могут полностью защитить слизистую оболочку ЖКТ от «атаки» грибов, но благодаря собственной «киллерной» субстанции через специфический механизм запускают активацию комплемента, который усиливает фагоцитоз. Следует отметить, что фагоцитоз особенно важен при кандидозной инфекции, но «не работает» в тканях против капсулированных криптококков и большинства мицелиальных грибов.
Нормальные биохимические, гистохимические и физиологические процессы в ЖКТ, своевременная регенерация эпителиоцитов, кислотно-ферментативный барьер, полноценная перистальтическая активность также являются защитными факторами, которые препятствуют проникновению грибковой и бактериальной флоры [4]. Роль желудочной кислоты в предотвращении внедрения грибов в слизистую неоспорима. В среде с пониженной кислотностью грибы Candida приобретают патогенные свойства, появляются вегетирующие формы, образуется псевдомицелий или мицелий, повреждающий слизистую оболочку. У ВИЧ-инфицированных лиц, для которых характерна ахлоргидрия, попадающие с пищей грибы Candida могут вызывать кандидоз желудка, в то время как у людей с нормальным иммунитетом эта локализация встречается редко. Роль кислотности желудочного сока в развитии бактериальной и грибковой инфекции кишечника не подтверждена.
Облигатные микроорганизмы желудка и кишечника (аэробные лактобациллы, анаэробные бифидум-бактерии, нормальная кишечная палочка и др.) также играют защитную роль. Применение антибиотиков убивает, наряду с патогенными, и эти «полезные» бактерии, открывая на слизистой оболочке рецепторы адгезии для грибов [2].
Нельзя не упомянуть также о Helicobacter pylori, который довольно часто обитает в желудке, вызывает гастрит, язвенную болезнь, а иногда оказывает канцерогенное воздействие. В свою очередь, лечение хеликобактериоза антибиотиками приводит к активации грибов Candida и кандидозу желудка [1]. Ассоциации грибов с Helicobacter pylori и другими бактериями в ЖКТ встречаются нередко, что требует продуманного адекватного подхода к тактике лечения.
В желудке могут также присутствовать Saccharomyces cerevisiae и некоторые виды Candida, способные сбраживать и ферментировать до винного спирта сахара, попадающие с пищей в желудок. Этот феномен называется синдромом «пивоваренного завода» [14].
Вирулентность грибов, патогенные факторы, как и полисахариды (маннаны), плазмокоагулаза, эндотоксины, липиды, глюкоконъюгаты, влияют на развитие заболевания. Даже от внутривидовых способностей грибов зависит, разовьются ли в каждом конкретном случае кандиданосительство или болезнь [13]. Например, серотип В Candida albicans считается более вирулентным и наиболее распространенным возбудителем орофарингеального кандидоза у ВИЧ-инфицированных больных, также он поражает генитоуринарную систему и нередко выделяется из зева у гомосексуалистов.
Микроскопически факторы агрессии грибов Candida проявляются формированием ростковых трубок, псевдогифов и истинного мицелия — за счет них грибы могут врастать в стенку фагоцитов. Однако дрожжи, которые не способны продуцировать мицелий, такие, как Candida glabrata, Cryptococcus neoformans, также могут вызывать заболевания ЖКТ.
Диагностика
Тщательное изучение анамнеза, выявление факторов риска, хронических заболеваний ЖКТ, патогномоничных клинических симптомов играют большую роль в своевременности установления диагноза.
В последние годы за счет эндоскопических технологий расширились возможности диагностики грибкового эзофагита и гастрита. При эзофагогастродуоденоскопии обращают внимание на гиперемию и изъязвления слизистой, наличие белых налетов и «пленок», сужение просвета пищевода, скопление слизи. Во время этой процедуры в обязательном порядке следует брать материал для микробиологического исследования, так как не всегда этиология этих проявлений грибковая. Причем информативность исследования налетов выше, чем биоптатов (95% по сравнению с 39%).
Особенно перспективны видеоинформационные эндоскопические исследования с цифровой регистрацией и анализом изображения. Четкое разграничение неизмененных и патологических тканей, анализ гистохимических процессов в слизистой оболочке пищеварительного тракта возможны с помощью эндоскопической спектроскопии и флюоресцентной эндоскопии. Видео- и колоноскопия, хромоэндоскопия на фоне «лекарственного» сна по технологии «Диантек» имеют высокое качество исследования, безболезненность манипуляций и отсутствие стресса и страха у пациентов.
Следует, однако, подчеркнуть, что инвазивные манипуляции при воспаленной слизистой ЖКТ небезопасны, могут способствовать грибковой и бактериальной диссеминации, а иногда приводят к травме и перфорации стенки пищевода или желудка. Эндоскопическая ультрасонография с допплеровским картированием, контрастным усилением тканевых и сосудистых структур перспективна, она позволяет детально дифференцировать все слои стенки пищеварительного тракта. Неинвазивные методы — виртуальная эндоскопия, позволяющая получить трехмерное изображение, магнитно-резонансное исследование — имеют большое будущее [3].
Изучение гастродуоденальной моторики с помощью сцинтиграфии и электрогастрографии также важно для диагностики и назначения дополнительных лекарственных средств, так как нарушение двигательной функции желудка, «застой» в ЖКТ создают условия для размножения грибов и бактерий. Колоноскопия дает возможность оценить состояние слизистой кишечника, наличие белого налета, язвенных дефектов и т. д. В перспективе в гастроэнтерологии будут внедряться методы, в основе которых лежат новые научно-практические исследования: иммуноферментный анализ фекальных антигенов, ПЦР и даже генетическое тестирование [3].
Еще одним достаточно информативным методом в гастроэнтерологии является рентгенография пищевода, желудка и кишечника. Она дает возможность выявить дефекты наполнения (депо бария), изъязвления, деформацию, конвергенцию складок, изменения контуров и глубины перистальтики, сужение или расширение пищеводной трубки. С помощью рентгенографии желудка можно оценить его моторику, своевременность эвакуации пищевого комка, что важно для понимания патогенеза заболевания.
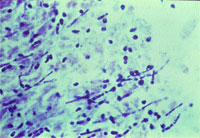 |
| Рисунок 1. Кандидозный эзофагит. Почкующиеся клетки и псевдогифы грибов Candida albicans на эзофагеальной язве |
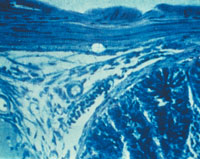 |
| Рисунок 2. Кандидозный энтерит. Утолщенные ворсинки и дефект слизистой тонкой кишки; псевдогифы грибов Candida |
Лабораторное подтверждение грибкового заболевания ЖКТ возможно при микроскопировании и/или культуральном исследовании смывов со слизистых оболочек полости рта и пищевода, содержимого желудка и кишечника, патологических «пленок», налетов и др. Количественная оценка грибов в биосубстратах должна проводиться в сопоставлении с клинической симптоматикой, с учетом наличия фоновых заболеваний, микст-инфекции и т. д. Например, обнаружение на слизистых единичных колоний Candida не является основанием для постановки диагноза «кандидоз» у иммунокомпетентных пациентов.
В кале диагностическую значимость приобретает количество колоний (более 10 5 –10 6 ). По-другому, с более низким диагностическим порогом, интерпретируются результаты посевов у иммуносупрессированных лиц, при нейтропении у больных СПИДом и в отделениях интенсивной терапии. Следует также обращать внимание на способность грибов к вегетации и образованию мицелия, так как это является одним из лабораторных признаков, подтверждающих диагноз кандидоза.
Гистологическое (окраска по Гомори–Гроккоту, ШИК-реакция) и цитологическое (окраска по Романовскому–Гимзе) исследования биоптатов позволяют обнаружить тканевые формы грибов. Многими авторами эти методы рассматриваются как наиболее достоверные. Кроме того, мицелий и псевдомицелий в тканях служат подтверждением наличия инвазивной формы грибковой инфекции ЖКТ (рис. 1, 2).
Кандидоз
Это наиболее распространенная грибковая оппортунистическая висцеральная патология. Агрессивные свойства грибов Candidа проявляются в их способности через стадию адгезии и инвазии поражать слизистые оболочки любых органов, в том числе и ЖКТ. Причем «атаке» подвергается чаще всего многослойный плоский эпителий полости рта и пищевода, реже — однослойный цилиндрический эпителий кишечника. Поэтому, как правило, в верхних отделах ЖКТ происходит инвазия грибов Candidа, а в отделах, расположенных ниже желудка, — колонизация. В то же время в кишечнике даже на стадии адгезии могут наблюдаться клинические симптомы — проявления неинвазивного кандидоза [10].
Язвенные дефекты пищевода, желудка и кишечника поддерживают грибковую колонизацию вплоть до инвазии. Желудочно-кишечный кандидоз нередко приводит к кандидемии.
Классификация кандидоза
I. Орофарингеальный кандидоз.
- Кандидоз полости рта у новорожденных.
- Псевдомембранозный кандидоз.
- Атрофический кандидоз полости рта (чаще у пожилых).
- Эритематозный кандидоз (новая форма).
- Срединный ромбовидный глоссит.
- Лейкоплакия, ассоциированная с кандидозом.
- Ангулярный кандидозный хейлит.
- Кандидозный гингивит (изолированно встречается редко).
II. Кандидозный эзофагит.
III. Кандидоз желудка.
- Эрозивно-фибринозный гастрит (диффузный).
- Вторичный кандидоз на фоне язвенной болезни.
- IV. Кандидоз кишечника.
- Псевдомембранозный.
- Коллагеновый.
- Лимфоцитарный.
V. Кандидозный проктосигмоидит.
VI. Перианальный кандидоз.
VII. Секреторная диарея, ассоциированная с кандидозом.
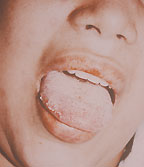 |
| Рисунок 3. Кандидозный глоссит. Типичные белые налеты и эрозии на воспаленной инфильтрированной слизистой |
Среди всех локализаций кандидоза пищеварительного тракта орофарингеальная занимает 1-е место (рис. 3).
О кандидозе полости рта упоминал еще Гиппократ, а впервые описал его хирург Лангенберк в 1839 г.
Кандидозный стоматит у новорожденных — распространенное заболевание. В первые дни после рождения слизистые ребенка устойчивы к грибам.
В дальнейшем недостаточная секреция IgA и постепенное снижение антимикробного иммунитета, переданного от матери, приводят к высокой заболеваемости. Патогномоничный синдром — белые творожистые налеты на слизистой полости рта, так называемая «молочница» [16].
Кандидоз ассоциирован также с ношением протезов. При этом развивается атрофический кандидоз, огромное количество грибов скапливается в щечных складках на фоне красного точечного воспаления слизистой; инвазия, как правило, отсутствует.
Кандидозный эзофагит в стационарах общего профиля встречается у 1,3–2,8% больных, в отделениях трансплантации — до 4%, при диссеминированном карциноматозе — от 2,8 до 6,7%. Это заболевание протекает часто без субъективных жалоб и выявляется случайно при «сплошных» исследованиях населения в 1–7% случаев [5, 17]. Иногда больные отмечают боль и дискомфорт при прохождении твердой и жидкой пищи, дисфагию, гиперсаливацию. По глубине поражения эндоскопически выделяют четыре типа — от легкого отека, гиперемии, единичных белых налетов
С. А. Бурова, доктор медицинских наук, профессор
Национальная академия микологии, ГКБ № 81, Москва
Источник



